FDS6690AS构成分子的原子是由原子核和电子组成
发布时间:2018/12/21 20:32:55 访问次数:428
众所周知,FDS6690AS 构成分子的原子是由原子核和电子组成,电子按一定的轨道在原子核外高速运动。其中,最外层电子比较活泼,可与邻近原子的外层 电子相互作用形成化学键。因此,电子,尤其是原子最外层电子,是分子中化学键的重要组成部分。原子核外电子的特性通常用电子轨道来描述,它包括电子运动轨迹(即电子云形状)和电子能量(轨道能级)两个最重要内涵。
当提到电子轨道时,既可以指原子中电子轨道,也可以指由原子构成的分子中的电子轨道。如果一个电子不属于任何一个原子核,则该电子为自由电子,其特征就不能用电子轨道来描述。原子内的电子通常具有波动性,服从测不准原理。也就是说,在分子、原子中运动的电子没有传统的运动轨道,而是行踪不定地按照一定概率在原子核附近空间出现。电子在原子核周围出现概率的空间分布称为电子云, 它反映出电子可能的运动空间,也称为电子轨道的形状。按照量子化学概念,原子中的电子轨道可以分为s、p、d、f四种,它们的电子云形状各不相同。
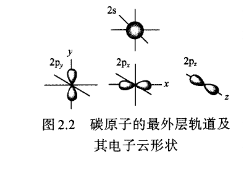
在有机材料中,碳是必不可少的元素。它是元素周期表中的第六号元素,共有6个电子,原子核外的电子可以表示为:1s铀/。图2,2表示的是孤立碳原子的最 外层4个电子的电子云分布。其中,s轨道具有球形对称性,可以在任何方向与其他原子成键。其他三个p轨道分别沿vz三个坐标轴的正负方向伸展,呈η”字形,因此与其他原子成键时,需要有一定的取向。
众所周知,FDS6690AS 构成分子的原子是由原子核和电子组成,电子按一定的轨道在原子核外高速运动。其中,最外层电子比较活泼,可与邻近原子的外层 电子相互作用形成化学键。因此,电子,尤其是原子最外层电子,是分子中化学键的重要组成部分。原子核外电子的特性通常用电子轨道来描述,它包括电子运动轨迹(即电子云形状)和电子能量(轨道能级)两个最重要内涵。
当提到电子轨道时,既可以指原子中电子轨道,也可以指由原子构成的分子中的电子轨道。如果一个电子不属于任何一个原子核,则该电子为自由电子,其特征就不能用电子轨道来描述。原子内的电子通常具有波动性,服从测不准原理。也就是说,在分子、原子中运动的电子没有传统的运动轨道,而是行踪不定地按照一定概率在原子核附近空间出现。电子在原子核周围出现概率的空间分布称为电子云, 它反映出电子可能的运动空间,也称为电子轨道的形状。按照量子化学概念,原子中的电子轨道可以分为s、p、d、f四种,它们的电子云形状各不相同。

在有机材料中,碳是必不可少的元素。它是元素周期表中的第六号元素,共有6个电子,原子核外的电子可以表示为:1s铀/。图2,2表示的是孤立碳原子的最 外层4个电子的电子云分布。其中,s轨道具有球形对称性,可以在任何方向与其他原子成键。其他三个p轨道分别沿vz三个坐标轴的正负方向伸展,呈η”字形,因此与其他原子成键时,需要有一定的取向。



 公网安备44030402000607
公网安备44030402000607





