��ƿ�ú�����編��簲ʱ��Ϊ��ƿ�����140%
����ʱ��:2023/3/27 13:09:17 ���ʴ���:86
���״̬���б�,��طŵ�ʱ,ֻ�ܷŵ��ŵ���ֹ��ѹ1��(����),����Ӱ���ص����������������ʱ(ָ��ƿ��λ���),Ϊ��֤���а�ȫ,��ر������,��Ҳ���ܳ�ʱ����䡣
���ڼ��Ե�ƿ�ĵ��Һ���μӻ�ѧ��Ӧ,���Һ���ػ�������,��˲�����Ǧ���ƿһ���ò������Һ���صķ������жϳ��״̬��
��ʵ��ʹ����,�������ó�������ʱ����ȷ����ƿ�Ƿ���㡣�������ĵ�ƿ�ú�����編���,���İ�ʱ����ԼΪ��ƿ�������140%��
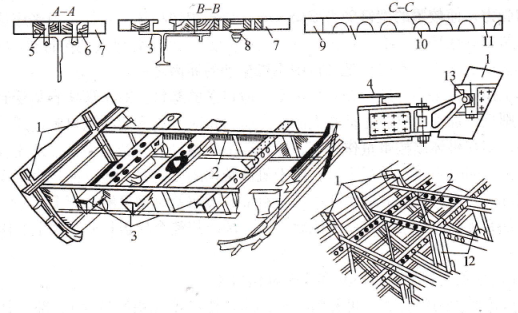
��������Һ������,�������طŵ�ʱ�Ļ�ѧ��Ӧԭ��ͼ
��ͨ��·��,������õ��Ӹ���������ĵ���,������Ļ�������N100H��ˮ�IJ�����,��������������Ni(0H)2������������0H����
������:2 Ni00H+2H20ʮ2e-��2 Ni(0H)2+20H��
�ڵ��Һ��,0H^�����缫Я�������Ǩ�Ƶ�������,��ɵ�ɴ��ݡ�
������:Cd+20H~�D)Cd(0H)2+2e
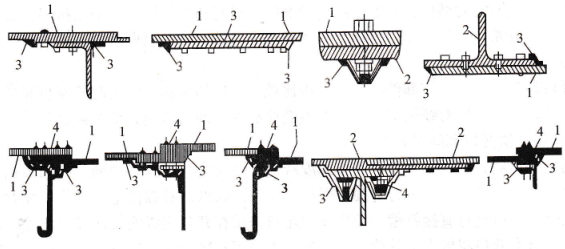
�������Ƿŵ���̵�����̡����������Դ����,ʹ���Ӵӵ�Դ�������,����Դ���ص�����,�������Ni(0H)2�ֻ�ԭΪNi00H,�������Cd(0H)2Ҳ�ָ�ΪCd��0H����
oH^�Ӹ���Ǩ��������,���Ѹ�����˻�����,��ɵ������á����ʱ��:
����:Cd(0H)2+2e-��Cd+20H��
IE|��: 2Ni (0H)2+20H~�D��2Ni00H+2H20+2c
�����Ϸ������Կ���,���ҺKOHû�в��뻯ѧ��Ӧ,�����˵������á�
�䡢�ŵ��ܵĻ�ѧ����ʽΪ:
2Ni(u)2+Cd(m)2u.2MH+(U)+2H20
����о��Ƽ�����˾http://xhkjgs.51dzw.com
���״̬���б�,��طŵ�ʱ,ֻ�ܷŵ��ŵ���ֹ��ѹ1��(����),����Ӱ���ص����������������ʱ(ָ��ƿ��λ���),Ϊ��֤���а�ȫ,��ر������,��Ҳ���ܳ�ʱ����䡣
���ڼ��Ե�ƿ�ĵ��Һ���μӻ�ѧ��Ӧ,���Һ���ػ�������,��˲�����Ǧ���ƿһ���ò������Һ���صķ������жϳ��״̬��
��ʵ��ʹ����,�������ó�������ʱ����ȷ����ƿ�Ƿ���㡣�������ĵ�ƿ�ú�����編���,���İ�ʱ����ԼΪ��ƿ�������140%��

��������Һ������,�������طŵ�ʱ�Ļ�ѧ��Ӧԭ��ͼ
��ͨ��·��,������õ��Ӹ���������ĵ���,������Ļ�������N100H��ˮ�IJ�����,��������������Ni(0H)2������������0H����
������:2 Ni00H+2H20ʮ2e-��2 Ni(0H)2+20H��
�ڵ��Һ��,0H^�����缫Я�������Ǩ�Ƶ�������,��ɵ�ɴ��ݡ�
������:Cd+20H~�D)Cd(0H)2+2e

�������Ƿŵ���̵�����̡����������Դ����,ʹ���Ӵӵ�Դ�������,����Դ���ص�����,�������Ni(0H)2�ֻ�ԭΪNi00H,�������Cd(0H)2Ҳ�ָ�ΪCd��0H����
oH^�Ӹ���Ǩ��������,���Ѹ�����˻�����,��ɵ������á����ʱ��:
����:Cd(0H)2+2e-��Cd+20H��
IE|��: 2Ni (0H)2+20H~�D��2Ni00H+2H20+2c
�����Ϸ������Կ���,���ҺKOHû�в��뻯ѧ��Ӧ,�����˵������á�
�䡢�ŵ��ܵĻ�ѧ����ʽΪ:
2Ni(u)2+Cd(m)2u.2MH+(U)+2H20

����о��Ƽ�����˾http://xhkjgs.51dzw.com
 �������
�������
- ��·ͼ������˺���������жϳ���·ͼ�źŴ���
- ECAM��EICAS�Ϻͼ�ʻ���ڿ�������Ͼ�
- ������ʱ�������ñ���������ż��ͨ��״̬��
- ��½����װ�ú�����ʽ����ܷɻ������˶��ȶ���
- ��ѹ�������������½�������Ͳ��ѹǻ����Ͳ�ڳ�
- ��С�¶ȵ��ڹ��̳������ڿ���ϵͳ�����¶ȱ仯
- �������ñ����������ܵ��ѱ��ʷ������������Ϲ�
- ��������Ԫ���õ����ȵĴ��й�����б������ú�
- ��ѹϵͳ��������ʱ���������豸�������ɻ��յ�
- �߱�����Ƶ���ʷŴ�����Դ��·��C�ͻ��ͱ�ѹ
 �Ƽ���������
�Ƽ���������
- ��Դ��ѹ������
- ���Ľ����S=34mm��60mm�� &nbs... [��ϸ]


 ��������44030402000607
��������44030402000607





